|
Reaksi Grignard
Reaksi Grignard (pengucapan /ɡriɲar/) adalah suatu reaksi kimia organologam yang mana alkil, vinil, atau aril-magnesium halida (pereaksi Grignard) ditambahkan ke dalam gugus karbonil dari suatu aldehida atau keton.[1][2] Reaksi ini adalah suatu cara penting untuk pembuatan ikatan karbon–karbon.[3][4] Reaksi antara suatu halida organik dengan magnesium bukan reaksi Grignard, tetapi menghasilkan pereaksi Grignard.[5] Reaksi dan pereaksi Grignard ditemukan oleh kimiawan Prancis François Auguste Victor Grignard (Universitas Nancy, Prancis), yang mendapat anugerah Nobel Kimia atas karyanya ini, dan namanya diabadikan sebagai nama reaksi dan pereaksi ini.[6] Pereaksi Grignard mirip dengan pereaksi organolitium karena keduanya merupakan nukleofil kuat yang dapat membentuk ikatan karbon–karbon baru. Mekanisme reaksiPereaksi Grignard berfungsi sebagai nukleofil, menyerang atom karbon elektrofil yang terdapat dalam ikatan polar gugus karbonil. Penambahan pereaksi Grignard pada karbonil biasanya berlangsung melalui suatu kondisi transisi cincin enam.[7]  Namun, tanpa pereaksi Grignard, reaksi dapat berlangsung dengan transfer elektron tunggal. Jalur serupa diasumsikan untuk reaksi lain pereaksi Grignard, contohnya, dalam pembentukan ikatan karbon–fosforus, karbon–timah, karbon–silikon, karbon–boron dan karbon–heteroatom lainnya. Preparasi pereaksi GrignardPereaksi Grignard dibuat melalui reaksi antara alkil atau aril halida dengan logam magnesium. Reaksi dilakukan dengan penambahan halida organik ke dalam suspensi magnesium dalam pelarut eter, yang menghasilkan ligan yang diperlukan untuk menstabilkan senyawa organomagnesium. Bukti empiris menunjukkan bahwa reaksi berlangsung pada permukaan logam. Reaksi berlangsung melalui transfer elektron tunggal:[8][9][10] Dalam reaksi pembentukan Grignard, radikal bebas dapat dikonversi menjadi karbanion melalui transfer elektron kedua.[11][12]
Keterbatasan pereaksi Grignard adalah bahwa mereka tidak segera bereaksi dengan alkil halida melalui mekanisme SN2. Di lain pihak, mereka segera mengendap melalui reaksi transmetalasi: Untuk kegunaan ini, pereaksi Grignard komersial sangat berguna karena dapat menghindari masalah pada tahap inisiasi.[13] Kondisi reaksiDalam reaksi yang melibatkan pereaksi Grignard, merupakan hal penting untuk menghindari air dan udara, yang dapat menghancurkan pereaksi dengan cepat melalui protonolisis atau oksidasi.[14] Oleh karena kebanyakan reaksi Grignard dilakukan dalam dietil ether atau tetrahidrofuran anhidrat, reaksi samping dengan udara dibatasi oleh selimut pelindung yang dihasilkan oleh uap pelarut. Preparasi skala kecil atau kuantitatif harus dilakukan dalam atmosfer nitrogen atau argon, menggunakan teknik bebas udara skipun pereaksi tetap perlu kering, ultrasonik dapat memungkinkan pembentukan pereaksi Grignard dalam pelarut basah dengan mengaktifkan magnesium sedemikian rupa sehingga ia mengkonsumsi air.[15] Halida organikReaksi Grignard sering kali dimulai dengan lambat. Sesuatu yang umum untuk reaksi yang melibatkan padatan dan larutan, inisiasi mengikuti suatu periode induksi selama magnesium reaktif terpapar pereaksi organik. Setelah periode induksi ini, reaksi dapat menjadi sangat eksotermik. Alkil dan aril bromida dan iodida umum digunakan, selain klorida. Namun, fluorida umumnya tidak reaktif, kecuali dengan magnesium aktif khusus. MagnesiumReaksi Grignard umum melibatkan penggunaan pita magnesium. Semua magnesium diselimuti lapisan magnesium oksida yang membuat pasif, yang menghambat reaksi dengan halida organik. Magnesium aktif khusus, seperti magnesium Rieke, memecahkan permasalahan ini.[16] Lapisan oksida dapat pula dipecahkan menggunakan ultrasonik,[17] atau dengan penambahan beberapa tetes iodium atau 1,2-Diiodoetana. Pelarut Sebagian besar reaksi Grignard dilakukan dalam pelarut eter, terutama dietil eter dan THF. Dengan pengkhelat dieter dioksan, beberapa pereaksi Grignard mengalami reaksi redistribusi menghasilkan senyawa diorganomagnesium (R = gugus organik, X = halida): Reaksi ini dikenal sebagai kesetimbangan Schlenk. Pengujian pereaksi GrignardOleh karena pereaksi Grignard sangat sensitif terhadap uap air dan oksigen, banyak metode yang telah dikembangkan untuk menguji mutu pereaksi. Pengujian yang biasa dilakukan melibatkan titrasi dengan penimbangan, pereaksi protik anhidrat, misalnya, mentol dengan adanya indikator warna. Interaksi pereaksi Grignard dengan fenantrolin[18] atau 2,2'-bipiridin menyebabkan perubahan warna. InisiasiBanyak metode telah dikembangkan untuk menginisiasi reaksi Grignard yang lamban. Metode ini melemahkan lapisan pasivator MgO, sehingga memapar magnesium yang sangat reaktif pada halida organik. Metode mekanis meliputi menghancurkan Mg berkeping-keping in situ, pengadukan cepat, dan sonikasi[19] suspensi. Iodium, metil iodida, dan 1,2-Dibromoetana adalah aktivator yang umum. Penggunaan 1,2-dibromoetana umumnya menguntungkan karena aksinya dapat dimonitor melalui observasi gelembung etilena. Lebih lanjut, produk sampingnya tidak berbahaya: Jumlah Mg yang dikonsumsi oleh zat pengaktif ini biasanya tidak signifikan. Sejumlah kecil merkuri klorida akan mengamalgamasi permukaan logam, sehingga memungkinkan terjadinya reaksi. Produksi skala industriPereaksi Grignard diproduksi secara industri untuk digunakan in situ, atau untuk diperjualbelikan. Sama seperti skala laboratorium, masalah utamanya terdapat pada tahap inisiasi; sebagian dari batch pereaksi Grignard sebelumnya sering digunakan sebagai inisiator. Reaksi Grignard bersifat eksotermik, dan eksotermisitas ini harus dipertimbangkan ketika skala reaksi ditingkatkan dari laboratorium ke skala pabrik.[20] Banyak pereaksi Grignard seperti metilmagnesium bromida, metilmagnesium klorida, fenilmagnesium bromida, dan alilmagnesium bromida tersedia secara komersial sebagai larutan tetrahidrofuran atau dietil eter. Reaksi transfer Mg (pertukaran halogen–Mg)Suatu alternatif preparasi pereaksi Grignard melibatkan transfer Mg dari pereaksi Grignard yang sudah diberi perlakuan kepada halida organik. Metode ini menawarkan keuntungan bahwa transfer Mg menoleransi banyak gugus fungsi. Umimnya reaksi ini melibatkan isopropilmagnesium klorida dan aril bromida atau iodida.[21] Reaksi pereaksi GrignardDengan senyawa karbonilPereaksi Grignard bereaksi dengan berbagai derivat karbonil.[22] 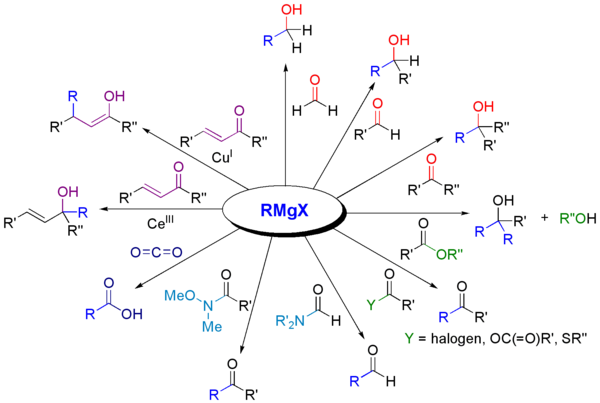 Aplikasi paling umum pereaksi Grignard adalah alkilasi aldehida dan keton, yaitu reaksi Grignard:[23]  Perlu diperhatikan bahwa gugus asetal (suatu karbonil terproteksi) tidak bereaksi. Reaksi semacam ini biasanya melibatkan kerja larutan asam akuatik, meskipun tahapan ini jarang ditunjukkan dalam skema reaksi. Dalam kasus di mana prreaksi Grignard ditambahkan kepada aldehida atau keton prokhiral, model Felkin-Anh atau aturan Cram biasanya dapat memprediksi stereoisomer yang akan terbentuk. Dengan 1,3-diketon dan substrat asam terkait yang mudah terdeprotonasi, pereaksi Grignard RMgX berfungsi sebagai basa, yang memberikan anion enolat dan membebaskan alkana RH. Pereaksi Grignard merupakan nukleofil dalam substitusi alifatik nukleofilik, misalnya dengan alkil halida dalam tahapan penentu pada produksi Naproksen industri: 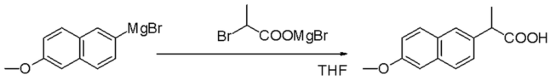  Reaksi sebagai basaPereaksi Grignard bertindak selaku basa untuk substrat protik (skema ini tidak menunjukkan kondisi sebenarnya, yang biasanya mengandung air). Pereaksi Grignard bersifat basa dan bereaksi dengan alkohol, fenol, dsb. untuk menghasilkan alkoksida (ROMgBr). Derivat fenoksida ditengarai mengalami formilasi paraformaldehida menghasilkan salisilaldehida.[24] Pembentukan ikatan dengan B, Si, P, SnSeperti senyawa organolitium, pereaksi Grignard berguna untuk pembentukan ikatan karbon–heteroatom.  Reaksi dengan halida logam transisiPereaksi Grignard bereaksi dengan banyak elektrofil berbasis logam. Contohnya, mereka mengalami transmetalasi dengan kadmium klorida (CdCl2) menghasilkan dialkilkadmium:[25] Pereaksi dialkilkadmium digunakan untuk preparasi keton dari asil halida: Dengan halida organikPereaksi Grignard tidak bereaksi dengan halida organik, berlawanan dengan golongan halida utama lainnya yang memiliki reaktivitas tinggi. Nsmun, dengan adanya katalis logam metal catalysts, pereaksi Grignard berperan dalam reaksi penggandengan C-C. Sebagai contoh, nonilmagnesium bromida bereaksi dengan metil p-klorobenzoate menghasilkan asam p-nonilbenzoat, dengan adanya Tris(asetilasetonato)besi(III) (Fe(acac)3), setelah direaksikan dengan NaOH untuk menghidrolisis ester, seperti terlihat di bawah. Tanpa Fe(acac)3, pereaksi Grignard akan menyerang gugus ester melalui aril halida.[26] 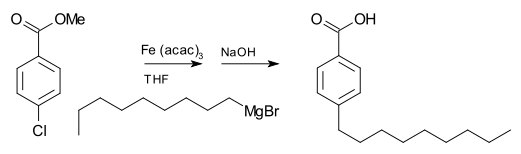 Untuk penggandengan aril halida dengan pereaksi aril Grignard, nikel klorida dalam tetrahidrofuran (THF) juga merupakan katalis yang baik. Sebagai tambahan, suatu katalis yang efektif untuk penggandengan alkil halida adalah dilitium tetraklorokuprat (Li2CuCl4), dibuat dengan mencampur litium klorida (LiCl) dan tembaga(II) klorida (CuCl2) dalam THF. Penggandengan Kumada-Corriu memberi akses kepada stirena [tersubstitusi]. OksidasiPerlakuan pereaksi Grignard dengan oksigen menghasilkan magnesium organoperoksida. Hidrolisis bahan ini menghasilkan hidroperoksida atau allohol. Reaksi ini melibatkan perantara radikal.
Oksidasi sederhana pereaksi Grignard untuk menghasilkan alkohol sedikit kurang praktis karena rendemen yang dihasilkan sedikit. Sebaliknya, urutan dua tahap melalui boran (vide supra) yang teroksidasi bertahap menjadi alkohol dengan hidrogen peroksida merupakan utilitas sintetik. Utilitas sintetis oksidasi Grignard dapat ditingkatkan dengan mereaksikan pereaksi Grignard dengan oksigen dengan keberadaan alkena menjadi alkohol berrantai etilena.[27] Modifikasi ini memerlukan aril atau vinil Grignard. Penambahan Grignard dan alkena saja tidak menghasilkan apa-apa dalam suatu reaksi yang menunjukkan bahwa kehadiran oksigen adalah esensial. Satu-satunya kelemahan adalah persyaratan minimal dua ekivalen Grignard meskipun ini sebagian dapat dielakkan dengan penggunaan sistem Grignard ganda dengan pereduksi Grignard yang murah seperti n-butilmagnesium bromida.  EliminasiDalam sintesis olefin Boord, penambahan magnesium pada β-haloeter tertentu menghasilkan alkena dalam reaksi eliminasi. Reaksi ini dapat membatasi penggunaan reaksi Grignard.  Degradasi pereaksi GrignardDalam waktu yang bersamaan, pembentukan dan hidrolisis pereaksi Grignard digunakan dalam penentuan jumlah atom halogen dalam senyawa organik.[28] Dalam penggunaan modern degradasi Grignard digunakan dalam analisis kimia triasilgliserol tertentu.[29] Penggunaan industriContoh reaksi Grignard merupakan langkah kunci dalam (non-stereospesifik) produksi industri Tamoksifen[30] (saat ini digunakan untuk pengobatan kanker payudara positif reseptor estrogen pada wanita):[31]  Galeri
Lihat pula
Referensi
Bacaan lebih lanjut
|
||||||||||||||













