|
Elektrode hidrogen standar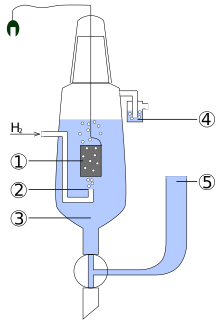 1. elektrode platina terplatinasi 2. gas hidrogen 3. larutan asam dengan aktivitas H+ = 1 mol/l 4. perapat hidro untuk mencegah gangguan oksigen 5. reservoir untuk menaruh setengah-elemen kedua dari sel galvani. Elektrode hidrogen standar (disingkat SHE), adalah suatu elektrode redoks yang menjadi dasar bagi skala termodinamika pada potensial reduksi-oksidasi.[1] Potensial elektrode absolutnya diperkirakan sebesar 4.44 ± 0.02 V pada 25 °C, tetapi untuk menjadi dasar bagi perbandingan dengan seluruh reaksi elektrode lainnya, potensial elektrode standar hidrogen (E0) disekapati bernilai nol volt hanya pada suhu 298K.[2] Potential dari elektrode lainnya dibandingkan dengan elektrode hidrogen standar pada suhu yang sama. Elektrode hidrogen didasarkan pada setengah-sel redoks:[3]
Reaksi redoks ini terjadi pada elektrode platina. Elektrode ini dicelupkan dalam suatu larutan asam dan gas hidrogen murni dialirkan di dalamnya.[4] Konsentrasi baik bentuk tereduksi dan teroksidasinya dijaga tetap sama. Hal ini menunjukkan bahwa tekanan gas hidrogen adalah 1 bar (100 kPa) dan aktivitas ion hidrogen dalam larutan tetap sama. Aktivitas ion hidrogen dalam konsentrasi efektifnya, yang sama dengan konsentrasi formal dikali koefisien aktivitasnya. Koefisien aktivitas tak-bersatuan ini mendekati 1,00 untuk larutan air yang sangat encer, tetapi biasanya lebih rendah bagi larutan yang lebih pekat.[5] Persamaan Nernst untuk reaksi diatas dapat dituliskan sebagai:[6] yang dalam persamaan di atas:
Lihat pulaWikimedia Commons memiliki media mengenai Elektrode hidrogen standar.
Referensi
Bacaan lebih lanjut
|

