Terbium(III) bromida
|
| Nama
|
| Nama lain
Terbium tribromida
|
| Penanda
|
|
|
|
|
|
|
| 3DMet
|
{{{3DMet}}}
|
| Nomor EC
|
|
|
|
|
| Nomor RTECS
|
{{{value}}}
|
|
|
|
InChI=1S/3BrH.Tb/h3*1H;/q;;;+3/p-3
|
|
|
| Sifat
|
|
|
TbBr3
|
| Massa molar
|
398,637 g/mol
|
| Penampilan
|
Bubuk Putih (heksahidrat)[1]
|
| Densitas
|
4,62 g/cm3[2]
|
| Titik lebur
|
827 °C (1.521 °F; 1.100 K)[4]
|
| Titik didih
|
1.490 °C (2.710 °F; 1.760 K)[3]
|
|
|
Larut[3]
|
| Bahaya
|
| Piktogram GHS
|

|
| Keterangan bahaya GHS
|
{{{value}}}
|
|
|
H315, H319, H335
|
|
|
P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501
|
| Senyawa terkait
|
|
|
Terbium(III) fluorida
Terbium(III) klorida
Terbium(III) iodida
|
|
|
Gadolinium(III) bromida
Disprosium(III) bromida
|
|
|
 N verifikasi (apa ini N verifikasi (apa ini  Y Y N ?) N ?)
|
| Referensi
|
|
|
|
Terbium(III) bromida (TbBr3) adalah sebuah senyawa anorganik berbentuk kristal.[5]
Produksi dan sifat
Terbium(III) bromida dapat diproduksi dengan memanaskan logam terbium atau terbium(III) oksida dengan amonium bromida.[6]
- Tb2O3 + 6 NH4Br → 2 TbBr3 + 6 NH3 + 3 H2O
Larutan terbium(III) bromida dapat mengkristalkan heksahidratnya. Saat dipanaskan, ia akan mengalami dehidrasi dan menghasilkan sejumlah TbOBr.[7]
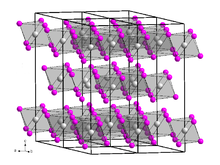
Terbium(III) bromida merupakan padatan berwarna putih yang dapat larut dalam air.[3] Struktur kristalnya sama seperti bismut iodida.[8]
Referensi
- ^ D. Brown, S. Fletcher, D. G. Holah (1968). "The preparation and crystallographic properties of certain lanthanide and actinide tribromides and tribromide hexahydrates". Journal of the Chemical Society A: Inorganic, Physical, Theoretical (dalam bahasa Inggris): 1889–1894. doi:10.1039/j19680001889. ISSN 0022-4944. Diakses tanggal 17 Februari 2024.
- ^ americanelements.com: Terbium Bromide
- ^ a b c CRC Handbook of Chemistry and Physics, Edisi ke-87, S. 4–94
- ^ Sigma-Aldrich Co., produk no. 466344.
- ^ "Terbium(III) bromide".
- ^ Gerd Meyer, Siegfried Dötsch, Thomas Staffel (Januari 1987). "The ammonium-bromide route to anhydrous rare earth bromides MBr3". Journal of the Less Common Metals (dalam bahasa Inggris). 127: 155–160. doi:10.1016/0022-5088(87)90372-9. Diakses tanggal 17 Februari 2024.
- ^ I. Mayer, S. Zolotov (September 1965). "The thermal decomposition of rare earth and yttrium bromide hydrates". Journal of Inorganic and Nuclear Chemistry (dalam bahasa Inggris). 27 (9): 1905–1909. doi:10.1016/0022-1902(65)80042-2. Diakses tanggal 17 Februari 2024.
- ^ Jean D'Ans, Ellen Lax (1997). Taschenbuch für Chemiker und Physiker. Springer DE. hlm. 1386. ISBN 354060035-3.
|
|---|
| Terbium(III) | |
|---|
| Terbium(III,IV) | |
|---|
| Terbium(IV) | |
|---|
Garam dan turunan kovalen dari ion bromida |
|---|
|

