|
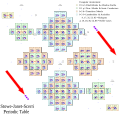
Tabel periodik alternatif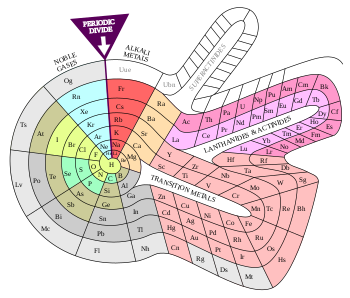 Tabel periodik alternatif adalah tabulasi unsur-unsur kimia yang berbeda secara signifikan dalam hal tata letaknya dibandingkan sistem periodik tradisional.[1][2] Beberapa telah dirancang, sering kali murni untuk alasan didaktika, karena tidak semua korelasi antara unsur kimia tertuang secara efektif pada tabel periodik standar. Tabel periodik alternatif dikembangkan sering kali dengan tujuan untuk menyoroti atau menekankan perbedaan sifat-sifat kimia atau fisika unsur-unsur, yang tidak tampak dalam tabel periodik tradisional. Beberapa tabel bertujuan untuk menekankan baik struktur inti maupun elektron atom. Hal ini bisa dilakukan dengan mengubah hubungan spasial atau representasi masing-masing unsur dengan unsur lain di dalam tabel. Tabel lain bertujuan untuk menekankan isolasi unsur kimia oleh manusia. Struktur alternatif utamaTabel periodik kidal (Janet, 1928)Tabel periodik kidal Charles Janet (1928)[3] dianggap menjadi alternatif yang paling signifikan untuk penggambaran sistem periodik tradisional. Ia menyusun unsur menurut pengisian orbital (bukan valensi) dan secara luas digunakan oleh fisikawan.[4]
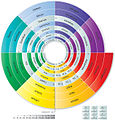
 Dibandingkan dengan tata letak umum, tabel kidal memiliki perubahan berikut:
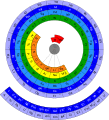
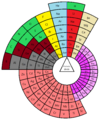
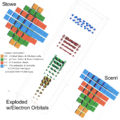
ADOMAH (2006) Sebuah versi kidal modern dibangun oleh Valery Tsimmerman, yang dikenal sebagai 'tabel periodik ADOMAH' (2006).[5] Strukturnya didasarkan pada empat bilangan kuantum konfigurasi elektron.[6] Spiral dua dimensi (Benfey, 1964)Dalam tabel periodik Theodor Benfey (1964), unsur-unsur membentuk suatu spiral dua dimensi, mulai dari hidrogen, dan melipat jalan mereka di sekitar dua peninsula, yang berisi logam transisi, dan lantanida serta aktinida. Sebuah pulau superaktinida telah pula dipetakan.[7] Galaksi Kimia (2004) disusun dengan cara yang sama. Tiga dimensi, fisikawan (Timmothy Stowe)Tabel periodik fisikawan Timmothy Stowe adalah tabel tiga dimensi dengan tiga sumbu mewakili bilangan kuantum utama, bilangan kuantum orbital, bilangan kuantum magnetik orbital. Helium lagi-lagi adalah unsur golongan 2. Tiga dimensi, seperti bunga (Paul Giguère, 1966)Tabel periodik 3-D Paul Giguère terdiri dari 4 papan iklan ((Inggris): billboard) berhubungan yang unsur-unsurnya ditulis pada bagian depan dan belakang. Billboard pertama memiliki unsur golongan 1 di bagian depan dan unsur golongan 2 di belakang, dengan menghilangkan hidrogen dan helium sama sekali. Pada sudut 90° billboard kedua berisi golongan 13-18 pada bagian depan dan belakang. Dua billboard selebihnya masing-masing membuat sudut 90° berisi unsur-unsur lainnya.[8][9] Pengulangan unsur (Ronald L. Rich, 2005)Ronald L. Rich telah mengusulkan tabel periodik di mana unsur muncul lebih dari sekali pada saat yang tepat.[10] Dia mencatat bahwa hidrogen berbagi sifat dengan unsur golongan 1 berdasarkan valensinya, dengan unsur golongan 17 karena hidrogen adalah nonlogam, dan juga dengan golongan karbon berdasarkan kesamaan dalam pembentukan ikatan kimia dengan logam transisi sera kemiripan elektronegativitasnya. Dalam penyajian tabel periodik ini, karbon dan silikon juga muncul dalam golongan yang sama dengan titanium dan zirkonium. Lain-lainSebuah tabel kimiawan (Newlands Revisited) dengan suatu alternatif penempatan hidrogen, helium dan lanthanida dipublikasikan oleh EG Marks dan JA Marks pada tahun 2010.[11] Variasi tata letak klasikDari tabel periodik asli Mendeleev, unsur-unsur pada dasarnya telah disusun menurut valensi (golongan dalam kolom) dan pengulangan di dalamnya (periode dalam baris). Selama bertahun-tahun dan dengan penemuan struktur atom, skema ini telah disesuaikan dan diperluas, tetapi tidak berubah secara prinsip.  Tabel periodik tertua adalah tabel bentuk pendek (kolom I–VIII) oleh Dmitri Mendeleev, yang menunjukkan kekerabatan kimia sekunder. Sebagai contoh, logam alkali dan logam mata uang (tembaga, perak, emas) berada di golongan yang sama karena kedua kelompok cenderung memiliki valensi satu. Format ini masih digunakan oleh banyak orang, seperti ditunjukkan oleh tabel kontemporer Rusia bentuk pendek Diarsipkan 2013-12-17 di Wayback Machine. ini, yang mencakup semua unsur dan nama unsur hingga roentgenium. H.G. Deming menggunakan istilah tabel periodik panjang (18 kolom) dalam buku teksnya General Chemistry, yang beredar di AS untuk pertama kalinya pada tahun 1923 (Wiley), dan yang pertama memberi notasi "A" untuk dua golongan awal dan lima golongan terakhir pada Golongan Utama, dan Golongan Transisi yang ada di tengah diberi notasi "B". Penomoran dipilih sedemikian rupa sehingga karakteristik oksida golongan B akan sesuai dengan yang ada di golongan A. Golongan besi, kobalt, dan nikel tidak termasuk Golongan A maupun B. Golongan gas mulia sejatinya dicantumkan (oleh Deming) pada sisi kiri tabel periodik. Golongan ini kemudian dialihkan ke sisi kanan dan biasanya diberi label sebagai Golongan VIIIA. Tabel periodik perluasan (extended periodic table)Dalam tabel periodik perluasan, diusulkan oleh Glenn T. Seaborg pada tahun 1969, unsur-unsur yang belum diketahui sudah dimasukkan hingga nomor atom 218. Ditambahkan periode teoretis di atas periode reguler 7. Dalam penelitian di bidang superatom, gugusan atom memiliki sifat-sifat atom tunggal unsur-unsur lainnya. Diusulkan untuk memperluas tabel periodik dengan lapisan kedua untuk diisi dengan gugus senyawa ini. Penambahan terakhir pada tabel multikisah ini adalah gugus ion aluminium Al−7, yang berperilaku layaknya atom multivalen germanium.[12] Galeri
Referensi
Sumber lain
Pranala luar
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||