|
Penghambat penyerapan kembali serotonin-norepinefrin
Penghambat penyerapan kembali serotonin-norepinefrin (Bahasa Inggiris: Serotonin–norepinephrine reuptake inhibitor, disingkat SNRI) adalah golongan obat antidepresan yang digunakan untuk mengobati gangguan depresi mayor (MDD), gangguan kecemasan, fobia sosial, nyeri neuropatik kronis, sindrom fibromialgia (FMS), dan gejala menopause. Penggunaan di luar label meliputi pengobatan untuk gangguan pemusatan perhatian dan hiperaktivitas (ADHD), dan gangguan obsesif kompulsif (OCD).[1] SNRI adalah penghambat penyerapan kembali monoamina; khususnya mereka menghambat penyerapan kembali serotonin dan norepinefrin. Neurotransmiter ini dianggap memainkan peran penting dalam pengaturan suasana hati. SNRI dapat dikontraskan dengan penghambat penyerapan kembali serotonin selektif (SSRI) dan penghambat penyerapan kembali norepinefrin (NRI), yang bekerja pada neurotransmiter tunggal.[2] Pengangkut serotonin manusia (SERT) dan pengangkut norepinefrin (NAT) adalah protein transpor membran yang bertanggung jawab atas penyerapan kembali serotonin dan noradrenalin dari celah sinaptik kembali ke terminal saraf presinaptik. Penghambatan ganda penyerapan kembali serotonin dan noradrenalin dapat memberikan keuntungan dibandingkan obat antidepresan lain dengan mengobati berbagai gejala yang lebih luas.[3] Obat-obatan ini dapat sangat berguna untuk nyeri kronis atau neuropatik yang terjadi bersamaan.[4] SNRI, bersama dengan SSRI dan NRI, adalah antidepresan generasi kedua. Sejak diperkenalkan pada akhir tahun 1980-an, antidepresan generasi kedua sebagian besar telah menggantikan antidepresan generasi pertama, seperti antidepresan trisiklik (TCA) dan penghambat oksidase monoamina (MAOI), sebagai obat pilihan untuk pengobatan MDD karena tolerabilitas dan profil keamanannya yang lebih baik.[5] SejarahPada tahun 1952, iproniazid, suatu agen antimikobakteri, ditemukan memiliki sifat psikoaktif saat diteliti sebagai pengobatan yang mungkin untuk tuberkulosis. Para peneliti mencatat bahwa pasien yang diberi iproniazid menjadi ceria, lebih optimis, dan lebih aktif secara fisik. Segera setelah pengembangannya, iproniazid dan zat terkait terbukti memperlambat pemecahan enzimatik serotonin, dopamin, dan norepinefrin melalui penghambatan enzim oksidase monoamina. Karena alasan ini, kelas obat ini dikenal sebagai penghambat oksidase monoamina (MAOI). Selama waktu ini pengembangan agen antidepresan yang sangat berbeda juga diteliti. Imipramin menjadi antidepresan trisiklik (TCA) pertama yang berguna secara klinis. Imipramin ditemukan memengaruhi banyak sistem neurotransmiter dan menghalangi penyerapan kembali norepinefrin dan serotonin dari sinapsis, sehingga meningkatkan kadar neurotransmiter ini. Penggunaan MAOI dan TCA memberikan kemajuan besar dalam pengobatan depresi, tetapi penggunaannya dibatasi oleh efek samping yang tidak menyenangkan dan masalah keamanan dan toksisitas yang signifikan.[6] Sepanjang tahun 1960-an dan 1970-an, hipotesis katekolamina tentang emosi dan hubungannya dengan depresi menjadi perhatian luas dan bahwa penurunan kadar neurotransmiter tertentu seperti norepinefrin, serotonin, dan dopamin mungkin berperan dalam patogenesis depresi. Hal ini menyebabkan pengembangan fluoksetin, SSRI pertama. Profil keamanan dan tolerabilitas SSRI yang lebih baik pada pasien dengan MDD, dibandingkan dengan TCA dan MAOI, merupakan kemajuan penting lainnya dalam pengobatan depresi.[6] Sejak akhir tahun 1980-an, SSRI telah mendominasi pasar obat antidepresan. Saat ini, ada peningkatan minat pada obat antidepresan dengan mekanisme aksi yang lebih luas yang dapat menawarkan peningkatan dalam kemanjuran dan tolerabilitas. Pada tahun 1993, obat baru diperkenalkan ke pasar AS yang disebut venlafaksin, suatu penghambat penyerapan kembali serotonin-norepinefrin.[7] Venlafaksin adalah senyawa pertama yang dideskripsikan dalam kelas baru zat antidepresan yang disebut feniletilamin. Zat-zat ini tidak terkait dengan TCA dan SSRI lainnya. Venlafaksin memblokir penyerapan kembali neuronal serotonin, noradrenalin; dan pada tingkat yang lebih rendah, dopamin di sistem saraf pusat. Berbeda dengan beberapa obat antidepresan lainnya, venlafaksin dapat menginduksi onset aksi yang cepat terutama karena penghambatan penyerapan kembali norepinefrin berikutnya.[8] Lihat garis waktu pada gambar 1.  Medikasi Ada delapan SNRI yang disetujui FDA di Amerika Serikat, dengan venlafaksin menjadi obat pertama yang dikembangkan pada tahun 1993 dan levomilnacipran menjadi obat terbaru yang dikembangkan pada tahun 2013. Obat-obatan tersebut bervariasi berdasarkan penggunaan medis lainnya, struktur kimia, efek samping, dan kemanjurannya.[9]
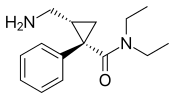
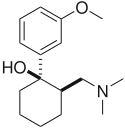
Mekanisme kerjaMonoamina dihubungkan dengan patofisiologi depresi. Gejala dapat terjadi karena konsentrasi neurotransmiter, seperti norepinefrin dan serotonin, tidak mencukupi, yang menyebabkan perubahan hilir.[13][25] Obat untuk depresi memengaruhi transmisi serotonin, norepinefrin, dan dopamin.[13] Antidepresan yang lebih lama dan kurang selektif seperti TCA dan MAOI menghambat penyerapan kembali atau metabolisme norepinefrin dan serotonin di otak, yang menghasilkan konsentrasi neurotransmiter yang lebih tinggi.[25] Antidepresan yang memiliki mekanisme kerja ganda menghambat penyerapan kembali serotonin dan norepinefrin, dan dalam beberapa kasus menghambat dengan efek yang lemah pada penyerapan kembali dopamin.[13] Antidepresan memengaruhi reseptor neuronal variabel seperti kolinergik muskarinik, adrenergik α1 dan α2, histaminergik H1, dan saluran natrium di otot jantung, yang menyebabkan penurunan konduksi jantung dan kardiotoksisitas yang khususnya terkait dengan TCA, dan pada tingkat yang lebih rendah dengan SSRI.[26] Selektivitas agen antidepresan didasarkan pada neurotransmiter yang dianggap memengaruhi gejala depresi.[27] Obat yang secara selektif memblokir penyerapan kembali serotonin dan norepinefrin secara efektif mengobati depresi dan ditoleransi lebih baik daripada TCA. TCA memiliki efek komprehensif pada berbagai reseptor neurotransmiter, yang menyebabkan kurangnya tolerabilitas dan peningkatan risiko toksisitas.[2] Antidepresan trisiklik Antidepresan trisiklik (TCA) adalah obat pertama yang memiliki mekanisme kerja ganda. Mekanisme kerja antidepresan amina sekunder trisiklik hanya dipahami sebagian. TCA memiliki efek penghambatan ganda pada transporter penyerapan kembali norepinefrin dan transporter penyerapan kembali serotonin. Peningkatan konsentrasi norepinefrin dan serotonin diperoleh dengan menghambat kedua protein transporter ini. TCA memiliki afinitas yang jauh lebih besar terhadap protein penyerapan kembali norepinefrin daripada SSRI. Hal ini karena pembentukan metabolit amina sekunder TCA.[28][29] Selain itu, TCA berinteraksi dengan reseptor adrenergik. Interaksi ini tampaknya penting untuk peningkatan ketersediaan norepinefrin di dalam atau di dekat celah sinaptik. Tindakan antidepresan trisiklik mirip imipramin memiliki adaptasi sekunder yang kompleks terhadap tindakan awal, dan berkelanjutannya sebagai penghambat transportasi norepinefrin, dan blokade variabel transportasi serotonin. Norepinefrin berinteraksi dengan subtipe reseptor adrenergik α dan β postsinaptik dan autoreseptor α2 presinaptik. Reseptor α2 mencakup autoreseptor presinaptik yang membatasi aktivitas neurofisiologis neuron noradrenergik di sistem saraf pusat. Pembentukan norepinefrin dikurangi oleh autoreseptor melalui enzim tirosin hidroksilase yang membatasi laju, efek yang dimediasi oleh penurunan fosforilasi-aktivasi enzim yang dimediasi oleh siklik AMP.[29] Reseptor α2 juga menyebabkan penurunan ekspresi siklik AMP intraseluler yang mengakibatkan relaksasi otot polos atau penurunan sekresi.[30] TCA mengaktifkan mekanisme umpan balik negatif melalui efeknya pada reseptor presinaptik. Satu kemungkinan penjelasan untuk efek pada penurunan pelepasan neurotransmitter adalah bahwa saat reseptor aktif terjadi penghambatan pelepasan neurotransmiter (termasuk penekanan arus Ca2+ yang bergantung pada tegangan, dan aktivasi arus K+ yang dioperasikan oleh reseptor yang digabungkan dengan protein G). Paparan berulang terhadap agen dengan jenis mekanisme ini menyebabkan penghambatan pelepasan neurotransmiter, tetapi pemberian TCA berulang akhirnya menyebabkan penurunan respons oleh reseptor α2. Desensitisasi respons ini mungkin disebabkan oleh peningkatan paparan norepinefrin endogen, atau dari okupasi mekanisme transpor norepinefrin yang berkepanjangan (melalui efek alosterik). Adaptasi ini memungkinkan sintesis dan sekresi norepinefrin presinaptik untuk kembali ke (atau bahkan melebihi) kadar norepinefrin normal di celah sinaptik. Secara keseluruhan, penghambatan penyerapan kembali norepinefrin yang diinduksi oleh TCA menyebabkan penurunan laju penembakan neuron (dimediasi melalui autoreseptor α2), aktivitas metabolik, dan pelepasan neurotransmiter.[29] TCA tidak secara langsung menghalangi transportasi dopamin, tetapi mungkin memfasilitasi efek dopaminergik secara tidak langsung dengan menghambat transportasi dopamin ke terminal noradrenergik korteks otak besar.[29] Karena mempengaruhi banyak reseptor yang berbeda, TCA memiliki efek samping, tolerabilitas yang buruk, dan peningkatan risiko toksisitas.[2] Penghambat penyerapan kembali serotonin selektifPenghambat penyerapan kembali serotonin selektif (SSRI) secara selektif menghambat penyerapan kembali serotonin dan merupakan kelompok antidepresan yang banyak digunakan.[31] Dengan peningkatan selektivitas reseptor dibandingkan dengan TCA, efek yang tidak diinginkan seperti tolerabilitas yang buruk dapat dihindari.[29] Serotonin disintesis dari asam amino yang disebut L-triptofan. Sistem transpor aktif mengatur penyerapan triptofan melintasi sawar darah otak. Jalur serotonergik diklasifikasikan menjadi dua jalur utama di otak: proyeksi menaik dari raphe medial dan dorsal dan proyeksi menurun dari raphe kaudal ke sumsum tulang belakang. Penghambat penyerapan kembali norepinefrin selektifNeuron noradrenergik terletak di dua wilayah utama di otak. Wilayah ini adalah locus coeruleus dan tegmental lateral. Dengan pemberian SNRI, aktivitas neuronal di daerah locus coeruleus diinduksi karena peningkatan konsentrasi norepinefrin di celah sinaptik. Hal ini mengakibatkan aktivasi reseptor adrenergik α2,[25] seperti yang dibahas sebelumnya. Pengujian telah menunjukkan bahwa SNRI memiliki kecenderungan yang tidak signifikan terhadap reseptor mACh, adrenergik α1 dan α2, atau H1.[27] Penghambat penyerapan kembali serotonin dan norepinefrin gandaAgen dengan penghambatan penyerapan kembali serotonin dan norepinefrin ganda terkadang disebut penghambat penyerapan kembali serotonin dan norepinefrin non-trisiklik. Studi klinis menunjukkan bahwa senyawa yang meningkatkan konsentrasi norepinefrin dan serotonin di celah sinaptik lebih berhasil daripada agen kerja tunggal dalam pengobatan depresi, tetapi data tersebut tidak meyakinkan apakah SNRI merupakan pilihan pengobatan yang lebih efektif daripada SSRI untuk depresi.[32][33][34] SNRI non-trisiklik memiliki beberapa perbedaan penting yang didasarkan pada farmakokinetika, metabolisme menjadi metabolit aktif, penghambatan isoform CYP, efek interaksi obat-obat, dan waktu paruh SNRI non-trisiklik.[28][35] Kombinasi mekanisme aksi dalam satu agen aktif merupakan perkembangan penting dalam psikofarmakologi.[35] Hubungan aktivitas strukturPerancah ariloksipropanaminaBeberapa penghambat penyerapan kembali mengandung perancah ariloksipropanamina. Motif struktural ini berpotensi untuk mengikat afinitas tinggi pada transpor amina biogenik.[35] Obat yang mengandung perancah ariloksipropanamina memiliki profil selektivitas untuk transporter norepinefrin dan serotonin yang bergantung pada pola substitusi cincin ariloksi. NRI selektif mengandung substituen pada posisi 2' dari cincin ariloksi, tetapi SSRI mengandung substituen pada posisi 4' dari cincin ariloksi. Atomoksetin, nisoksetin, dan reboksetin semuanya memiliki gugus substitusi pada posisi 2' dan merupakan NRI selektif, sementara senyawa yang memiliki gugus substitusi pada posisi 4' (seperti fluoksetin dan paroksetin) merupakan SSRI. Duloksetin mengandung gugus fenil yang menyatu pada posisi 2' dan 3', oleh karena itu ia memiliki efek penghambatan penyerapan kembali norepinefrin dan serotonin selektif ganda dan memiliki potensi yang sama untuk kedua transporter.[36] Sifat substituen aromatik juga memiliki pengaruh yang signifikan terhadap aktivitas dan selektivitas senyawa sebagai penghambat transporter serotonin atau norepinefrin.[35]  Perancah sikloalkanol metilaminVenlafaksin dan desvenlafaksin mengandung perancah sikloalkanol metilamin. Peningkatan sifat penarik elektron dari cincin aromatik memberikan efek penghambatan yang lebih kuat terhadap penyerapan norepinefrin dan meningkatkan selektivitas norepinefrin terhadap transporter serotonin. Efek substituen kloro, metoksi, dan trifluorometil dalam cincin aromatik perancah sikloalkanol metilamin diuji. Hasil penelitian menunjukkan bahwa analog m-trifluorometil penarik elektron terkuat menunjukkan efek penghambatan norepinefrin yang paling kuat dan selektivitas tertinggi terhadap penyerapan serotonin.[36] WY-46824, turunan yang mengandung piperazina, telah menunjukkan penghambatan penyerapan kembali norepinefrin dan dopamin. Sintesis dan pengujian lebih lanjut mengidentifikasi WAY-256805, penghambat penyerapan kembali norepinefrin kuat yang menunjukkan selektivitas yang sangat baik dan berkhasiat pada model hewan yang mengalami depresi, nyeri, dan disfungsi termoregulasi.[37]  Milnacipran Milnacipran secara struktural berbeda dari SNRI lainnya.[28] Hubungan struktur aktivitas turunan milnacipran pada tingkat transporter masih belum jelas dan didasarkan pada efikasi in vivo yang dilaporkan pada tahun 1987. N-metilasi milnacipran pada kelompok substituen R4 dan R5 mengurangi aktivitas norepinefrin dan serotonin. Penelitian pada berbagai amida sekunder pada kelompok substitusi R6 dan R7 menunjukkan bahwa elektron π memainkan peran penting dalam interaksi antara transporter dan ligan. Kelompok fenil pada substituen R6 menunjukkan efek pada transporter norepinefrin. Kelompok substituen pada R6 dan R7 dengan ikatan rangkap alilik menunjukkan peningkatan efek yang signifikan pada transporter norepinefrin dan serotonin.[38] Studi menunjukkan bahwa dengan memasukkan kelompok 2-metil pada substituen R3, potensi pada transporter norepinefrin dan serotonin hampir hilang. Kelompok metil dalam kelompok substituen R1 dan R2 juga menghilangkan potensi pada transporter norepinefrin dan serotonin. Para peneliti menemukan bahwa mengganti salah satu kelompok etil milnacipran dengan gugus alil meningkatkan potensi norepinefrin.[39] Farmakofor turunan milnacipran masih belum jelas.[38] Konformasi milnacipran merupakan bagian penting dari farmakofornya. Mengubah stereokimianya memengaruhi konsentrasi norepinefrin dan serotonin. Milnacipran dipasarkan sebagai campuran rasemat. Efek milnacipran berada pada isomer (1S,2R) dan substitusi gugus fenil pada isomer (1S,2R) berdampak negatif pada konsentrasi norepinefrin. Milnacipran memiliki berat molekul rendah dan lipofilitas rendah. Karena sifat-sifat ini, milnacipran menunjukkan farmakokinetika yang hampir ideal pada manusia seperti bioavailabilitas tinggi, variabilitas antar subjek rendah, interaksi enzim hati terbatas, distribusi jaringan sedang dan waktu paruh eliminasi cukup panjang. Kurangnya interaksi obat-obat melalui enzim sitokrom P450 pada milnacipran dianggap sebagai fitur yang menarik karena banyak obat sistem saraf pusat sangat lipofilik dan sebagian besar dieliminasi oleh enzim hati.[39] Pengembangan hubungan struktur aktivitas di masa mendatangPenerapan perancah ariloksipropanamina telah menghasilkan sejumlah MAOI yang poten.[40] Sebelum pengembangan duloksetin, eksplorasi hubungan struktur aktivitas ariloksipropanamina menghasilkan identifikasi fluoksetin dan atomoksetin. Motif yang sama dapat ditemukan dalam reboksetin yang dibatasi dalam sistem cincin morfolin. Beberapa penelitian telah dilakukan di mana oksigen dalam reboksetin digantikan oleh belerang untuk menghasilkan ariltiometil morfolin. Beberapa turunan ariltiometil morfolin mempertahankan kadar penghambatan penyerapan kembali serotonin dan norepinefrin yang poten. Penghambatan reuptake serotonin dan norepinefrin ganda berada dalam enantiomer yang berbeda untuk perancah ariltiometil morfolin.[41] Calon obat yang mungkin dengan aktivitas penghambatan penyerapan kembali serotonin dan norepinefrin ganda juga telah diturunkan dari templat piperazina, 3-amino-pirolidina, dan benzilamina.[42] Uji klinisDepresiBeberapa penelitian telah menunjukkan bahwa obat antidepresan yang menggabungkan aktivitas serotonergik dan noradrenergik umumnya lebih efektif daripada SSRI, yang bekerja pada penyerapan kembali serotonin dengan sendirinya. Obat antidepresan serotonergik-noradrenergik mungkin memiliki keunggulan efikasi yang sederhana dibandingkan dengan SSRI dalam mengobati gangguan depresi mayor (MDD),[43] tetapi sedikit kurang dapat ditoleransi dengan baik.[44] Penelitian lebih lanjut diperlukan untuk memeriksa kemungkinan perbedaan efikasi pada subpopulasi MDD tertentu atau untuk gejala MDD tertentu, antara kelas obat antidepresan ini. AnalgesikData dari uji klinis telah menunjukkan bahwa SNRI mungkin memiliki sifat meredakan nyeri. Meskipun persepsi dan transmisi rangsangan nyeri di sistem saraf pusat belum sepenuhnya dijelaskan, data yang luas mendukung peran serotonin dan norepinefrin dalam modulasi nyeri. Temuan dari uji klinis pada manusia telah menunjukkan bahwa antidepresan ini dapat membantu mengurangi nyeri dan gangguan fungsional pada kondisi nyeri sentral dan neuropatik. Properti SNRI ini dapat digunakan untuk mengurangi dosis obat pereda nyeri lain dan menurunkan frekuensi masalah keamanan, keterbatasan efikasi, dan tolerabilitas.[45] Data penelitian klinis telah menunjukkan pada pasien dengan GAD bahwa duloksetin secara signifikan lebih efektif daripada plasebo dalam mengurangi gejala nyeri terkait GAD, setelah pengobatan jangka pendek dan jangka panjang. Namun, temuan menunjukkan bahwa gejala nyeri fisik tersebut muncul kembali dalam situasi kambuh, yang menunjukkan perlunya pengobatan berkelanjutan pada pasien dengan GAD dan gejala fisik nyeri yang terjadi bersamaan.[46] IndikasiSNRI telah diuji untuk pengobatan kondisi berikut:
FarmakologiRute pemberian SNRI diberikan secara oral, biasanya dalam bentuk kapsul atau tablet. Dianjurkan untuk mengonsumsi SNRI di pagi hari bersama sarapan, yang tidak memengaruhi kadar obat, tetapi dapat membantu mengatasi efek samping tertentu.[48] Norepinefrin memiliki efek aktivasi dalam tubuh dan karenanya dapat menyebabkan insomnia pada beberapa pasien jika dikonsumsi sebelum tidur.[49] SNRI juga dapat menyebabkan mual, yang biasanya ringan dan hilang dalam beberapa minggu setelah pengobatan, tetapi mengonsumsi obat bersama makanan dapat membantu meredakannya.[50] Cara kerjaKondisi yang paling banyak diindikasikan untuk SNRI yakni gangguan depresi mayor, dianggap terutama disebabkan oleh penurunan kadar serotonin dan norepinefrin di celah sinaptik, yang menyebabkan sinyal tidak menentu. Namun teori tersebut telah dibantah.[51] Berdasarkan hipotesis monoamina depresi, yang menyatakan bahwa penurunan konsentrasi neurotransmiter monoamina menyebabkan gejala depresi, hubungan berikut ditentukan: "Norepinefrin mungkin terkait dengan kewaspadaan dan energi serta kecemasan, perhatian, dan minat dalam hidup; [kekurangan] serotonin dengan kecemasan, obsesi, dan kompulsi; dan dopamin dengan perhatian, motivasi, kesenangan, dan penghargaan, serta minat dalam hidup."[52] SNRI bekerja dengan menghambat penyerapan kembali neurotransmiter serotonin dan norepinefrin. Hal ini menghasilkan peningkatan konsentrasi ekstraseluler serotonin dan norepinefrin, akibatnya terjadi peningkatan neurotransmisi. Sebagian besar SNRI termasuk venlafaksin, desvenlafaksin, dan duloksetin, beberapa kali lipat lebih selektif untuk serotonin daripada norepinefrin, sementara milnacipran tiga kali lebih selektif untuk norepinefrin daripada serotonin. Peningkatan kadar norepinefrin dianggap perlu agar antidepresan efektif melawan nyeri neuropatik, suatu sifat yang dimiliki oleh antidepresan trisiklik (TCA) yang lebih lama, tetapi tidak dengan SSRI.[53] Penelitian terkini telah menunjukkan bahwa depresi dapat dikaitkan dengan peningkatan respons inflamasi,[54] sehingga upaya untuk menemukan mekanisme tambahan untuk SNRI telah dilakukan. Penelitian telah menunjukkan bahwa SNRI dan SSRI memiliki tindakan antiinflamasi yang signifikan pada mikroglia.[55] FarmakodinamikSebagian besar SNRI berfungsi bersama metabolit primer dan metabolit sekunder untuk menghambat penyerapan kembali serotonin, norepinefrin, dan sejumlah kecil dopamin. Misalnya, venlafaksin bekerja bersama metabolit primernya O-desmetilvenlafaksin untuk menghambat penyerapan kembali serotonin dan norepinefrin di otak. Bukti juga menunjukkan bahwa dopamin dan norepinefrin berperilaku dalam cara kotransportasi, karena inaktivasi dopamin oleh penyerapan kembali norepinefrin di korteks frontal, area otak yang sebagian besar kekurangan transporter dopamin. Efek SNRI ini menghasilkan peningkatan neurotransmisi dopamin, selain peningkatan aktivitas serotonin dan norepinefrin.[56] Lebih jauh, karena SNRI sangat selektif, SNRI tidak memiliki efek terukur pada reseptor lain yang tidak diinginkan, berbeda dengan penghambatan oksidase monoamina.[57] Pengujian farmasi telah menentukan bahwa penggunaan SNRI atau SSRI dapat menghasilkan tindakan antiinflamasi yang signifikan pada mikroglia.[55][19][58][59][14][60] Profil aktivitas
FarmakokinetikWaktu paruh venlafaksin adalah sekitar 5 jam, dan dengan dosis sekali sehari, konsentrasi keadaan tunak dicapai setelah sekitar 3 hari, meskipun metabolit aktifnya yakni desvenlafaksin bertahan lebih lama.[59] Waktu paruh desvenlafaksin adalah sekitar 11 jam, dan konsentrasi keadaan tunak dicapai setelah 4 hingga 5 hari.[58] Waktu paruh duloksetin adalah sekitar 12 jam (kisaran: 8–17 jam), dan keadaan tunak dicapai setelah sekitar 3 hari.[14] Milnacipran memiliki waktu paruh sekitar 6 hingga 8 jam, dan kadar keadaan tunak dicapai dalam 36 hingga 48 jam.[60] KontraindikasiSNRI dikontraindikasikan pada pasien yang mengonsumsi MAOI dalam dua minggu terakhir karena peningkatan risiko sindrom serotonin, yang dapat mengancam jiwa. Obat dan zat lain yang harus dihindari karena peningkatan risiko sindrom serotonin saat dikombinasikan dengan SNRI meliputi: antidepresan lain, antikonvulsan, analgesik, agen antiemetik, obat antimigrain, metilena biru, linezolid, Litium, St. John's wort, ekstasi, dan LSD.[64] Tanda dan gejala sindrom serotonin meliputi: hipertermia, kekakuan, mioklonus, ketidakstabilan otonom dengan tanda-tanda vital yang berfluktuasi, dan perubahan status mental yang meliputi agitasi ekstrem yang berkembang menjadi delirium dan koma.[14] Karena efek peningkatan kadar norepinefrin, dan oleh karena itu, aktivitas noradrenergik yang lebih tinggi, hipertensi yang sudah ada sebelumnya harus dikontrol sebelum pengobatan dengan SNRI dan tekanan darah dipantau secara berkala selama pengobatan.[65] Duloksetin juga dikaitkan dengan kasus gagal hati dan tidak boleh diresepkan kepada pasien dengan penggunaan alkohol kronis atau penyakit hati. Studi telah menemukan bahwa duloksetin dapat meningkatkan tes fungsi hati tiga kali lipat di atas batas normal atasnya.[66] Pasien dengan penyakit jantung koroner harus berhati-hati dalam penggunaan SNRI.[67] Lebih jauh lagi, karena beberapa tindakan SNRI terhadap obesitas, pasien dengan gangguan makan utama seperti anoreksia nervosa atau bulimia nervosa tidak boleh diresepkan SNRI.[19] Duloksetin dan milnacipran juga dikontraindikasikan pada pasien dengan glaukoma sudut sempit yang tidak terkontrol, karena telah terbukti meningkatkan kejadian midriasis.[14][60] Efek sampingKarena SNRI dan SSRI bekerja dengan cara yang sama untuk meningkatkan kadar serotonin, keduanya memiliki banyak efek samping meski dengan tingkat yang berbeda-beda. Efek samping yang paling umum meliputi mual/muntah, berkeringat, kehilangan nafsu makan, pusing, sakit kepala, peningkatan pikiran untuk bunuh diri, dan disfungsi seksual.[68] Peningkatan kadar norepinefrin terkadang dapat menyebabkan kecemasan, denyut nadi sedikit meningkat, dan tekanan darah tinggi. Namun antidepresan selektif norepinefrin seperti reboksetin dan desipramin telah berhasil mengobati gangguan kecemasan.[69] Orang yang berisiko hipertensi dan penyakit jantung harus memantau tekanan darah mereka.[19][58][59][14][60] Disfungsi SeksualSNRI dan SSRI dapat menyebabkan beberapa jenis disfungsi seksual seperti disfungsi ereksi, penurunan libido, anhedonia seksual, dan anorgasmia.[14][59][70] Dua efek samping seksual yang umum adalah berkurangnya minat terhadap seks (libido) dan kesulitan mencapai klimaks (anorgasmia), yang biasanya agak lebih ringan dengan SNRI dibandingkan dengan SSRI.[71] Untuk mengelola disfungsi seksual, penelitian telah menunjukkan bahwa beralih ke atau menambah bupropion atau menambahkan penghambat PDE5 telah mengurangi gejala disfungsi seksual. Penelitian telah menunjukkan bahwa penghambat PDE5 seperti sildenafil (Viagra), tadalafil (Cialis), vardenafil (Levitra), dan avanafil (Stendra) terkadang membantu mengurangi disfungsi seksual termasuk disfungsi ereksi, meski obat-obat tersebut telah terbukti lebih efektif pada pria daripada wanita.[72] Sindrom SerotoninEfek samping SNRI yang serius tetapi jarang terjadi adalah sindrom serotonin, yang disebabkan oleh kelebihan serotonin dalam tubuh. Sindrom serotonin dapat disebabkan oleh penggunaan beberapa obat serotonergik seperti SSRI atau SNRI. Obat lain yang berkontribusi terhadap sindrom serotonin meliputi MAOI, linezolid, tedizolid, metilena biru, prokarbazin, amfetamin, klomipramin, dan banyak lagi.[73] Gejala awal sindrom serotonin dapat meliputi mual, muntah, diare, berkeringat, agitasi, kebingungan, kekakuan otot, pupil melebar, hipertermia, kekakuan, dan bulu kuduk berdiri. Gejala yang lebih parah meliputi demam, sawan, detak jantung tidak teratur, delirium, dan koma.[74][75][14] Jika tanda atau gejala muncul, segera hentikan pengobatan dengan agen serotonergik.[74] Dianjurkan untuk mencuci 4 hingga 5 waktu paruh agen serotonergik sebelum menggunakan MAOI.[76] PerdarahanBeberapa penelitian menunjukkan adanya risiko perdarahan gastrointestinal bagian atas, terutama akibat dari venlafaksin, karena gangguan agregasi trombosit dan penipisan kadar serotonin trombosit.[77][78] Mirip dengan SSRI, SNRI dapat berinteraksi dengan antikoagulan seperti warfarin. Ada lebih banyak bukti bahwa SSRI memiliki risiko perdarahan yang lebih tinggi daripada SNRI.[77] Penelitian telah menyarankan kehati-hatian saat menggunakan SNRI atau SSRI dengan obat antiinflamasi nonsteroid (OAINS) dosis tinggi seperti ibuprofen atau naproksen karena peningkatan risiko perdarahan gastrointestinal bagian atas.[34] Masalah penglihatan Sama seperti antidepresan lainnya, obat SNRI diketahui menyebabkan sindrom salju visual (VSS), yakni suatu kondisi yang ditandai dengan gangguan penglihatan, palinopsia (negatif setelah melihat gambar), rabun senja (penglihatan buruk di malam hari), dan fotofobia (tampilan cahaya atau warna yang lebih terang). Bukti menunjukkan bahwa 8,9% dari mereka yang mengonsumsi SNRI mengalami salju visual; 10,5% mengalami palinopsia; 15,3% mengalami fotofobia; dan 17,7% mengalami niktolopia sebagai akibat dari asupan resep SNRI. Amitriptilin dan citalopram juga dilaporkan memperburuk atau menyebabkan gejala VSS.[79] Tindakan pencegahanMemulai regimen SNRIKarena perubahan ekstrem dalam aktivitas noradrenergik yang dihasilkan dari penghambatan penyerapan kembali norepinefrin dan serotonin, pasien yang baru memulai regimen SNRI biasanya diberikan dosis yang lebih rendah daripada dosis akhir yang diharapkan untuk memungkinkan tubuh menyesuaikan diri dengan efek obat. Saat pasien melanjutkan dengan dosis rendah tanpa efek samping, dosis ditingkatkan secara bertahap hingga pasien melihat perbaikan gejala tanpa efek samping yang merugikan.[80] Sindrom penghentianSeperti halnya SSRI, penghentian SNRI secara tiba-tiba biasanya menyebabkan putus obat, atau "sindrom penghentian", yang dapat mencakup keadaan cemas dan gejala lainnya. Oleh karena itu, disarankan bagi pengguna yang ingin menghentikan SNRI untuk secara perlahan mengurangi dosis harus di bawah pengawasan seorang profesional. Sindrom penghentian dilaporkan jauh lebih buruk pada venlafaksin jika dibandingkan dengan SNRI lainnya. Dengan demikian, karena tramadol berhubungan dengan venlafaksin, kondisi yang sama berlaku.[81] Hal ini kemungkinan besar disebabkan oleh waktu paruh venlafaksin yang relatif pendek, dan oleh karena itu pembersihannya cepat setelah penghentian. Dalam beberapa kasus, beralih dari venlafaksin ke fluoksetin, suatu SSRI kerja panjang, dan kemudian mengurangi fluoksetin, mungkin direkomendasikan untuk mengurangi gejala penghentian.[82][83] Tanda dan gejala putus obat dari penghentian SNRI secara tiba-tiba termasuk pusing, kecemasan, insomnia, mual, berkeringat, dan gejala seperti flu seperti kelesuan dan malaise.[83] OverdosisPenyebabOverdosis SNRI dapat disebabkan oleh kombinasi obat atau jumlah obat itu sendiri yang berlebihan. Venlafaksin sedikit lebih beracun jika overdosis daripada duloksetin atau SSRI.[19][58][59][14][60][84] GejalaGejala overdosis SNRI, baik itu interaksi obat campuran atau obat itu sendiri, bervariasi dalam intensitas dan kejadian berdasarkan jumlah obat yang diminum dan sensitivitas individu terhadap pengobatan SNRI. Gejala yang mungkin terjadi meliputi:[14]
PenangananOverdosis biasanya diobati secara simtomatik, terutama dalam kasus sindrom serotonin, yang memerlukan pengobatan dengan siproheptadin dan pengendalian suhu berdasarkan perkembangan toksisitas serotonin.[85] Pasien sering dipantau tanda-tanda vitalnya, dan saluran pernapasan dibersihkan untuk memastikan bahwa mereka menerima kadar oksigen yang cukup. Pilihan lain adalah menggunakan karbon aktif di saluran cerna untuk menyerap kelebihan neurotransmiter.[14] Perbandingan dengan SSRIKarena SNRI dikembangkan lebih baru daripada SSRI, jumlahnya relatif sedikit. Namun, SNRI termasuk antidepresan yang paling banyak digunakan saat ini. Pada tahun 2009, Cymbalta dan Effexor masing-masing adalah obat bermerek yang paling banyak diresepkan ke-11 dan ke-12 di Amerika Serikat. Ini berarti bahwa SNRI adalah antidepresan yang paling umum ke-2 dan ke-3, setelah Lexapro (escitalopram, suatu SSRI).[86] Dalam beberapa penelitian, SNRI menunjukkan efikasi antidepresan yang sedikit lebih tinggi daripada SSRI (tingkat respons 63,6% versus 59,3%).[43] Namun, dalam satu penelitian, escitalopram memiliki profil efikasi yang lebih unggul daripada venlafaksin.[87] Populasi khususKehamilanTidak ada antidepresan yang disetujui FDA selama kehamilan. Penggunaan antidepresan selama kehamilan dapat mengakibatkan kelainan pada janin yang memengaruhi perkembangan fungsional otak dan perilaku.[88] Penelitian telah menunjukkan korelasi antara wanita hamil yang diobati dengan SNRI dan risiko gangguan hipertensi,[89] preeklamsia,[90] keguguran,[91] sawan pada anak-anak,[92] dan banyak efek samping lainnya. PediatriSSRI dan SNRI telah terbukti efektif dalam mengobati gangguan depresi mayor dan kecemasan pada populasi anak-anak.[93] Namun, perbedaan dalam metabolisme, fungsi ginjal, serta persentase total air tubuh dan lemak tubuh dapat memengaruhi farmakokinetik obat-obatan pada remaja dibandingkan dengan orang dewasa.[94] Selain itu, ada risiko peningkatan keinginan bunuh diri pada populasi anak-anak untuk pengobatan gangguan depresi mayor, terutama dengan venlafaksin.[93] Fluoksetin dan Escitalopram adalah satu-satunya antidepresan yang disetujui untuk gangguan depresi mayor pada anak/remaja.[94] Tinjauan pustaka oleh Castagna, dkk. dari tahun 2023 menunjukkan indikasi kemanjuran dalam mengobati gangguan kecemasan umum pada anak. Saat ini, Duloksetin, sebuah SNRI, adalah satu-satunya obat yang disetujui FDA untuk GAD pada anak, meskipun faktanya SSRI biasanya merupakan pengobatan lini pertama.[94][95] Disarankan agar obat-obatan ini dikombinasikan dengan psikoterapi untuk memaksimalkan efektivitas.[96][94] GeriatriSebagian besar antidepresan, termasuk SNRI, aman dan efektif untuk populasi geriatri. Populasi geriatri berisiko lebih besar mengalami efek samping yang berkaitan dengan interaksi obat karena mereka lebih mungkin mengalami polifarmasi.[97] Keputusan sering kali didasarkan pada kondisi komorbiditas, interaksi obat, dan toleransi pasien. Karena perbedaan komposisi tubuh dan metabolisme, dosis awal sering kali setengah dari dosis yang direkomendasikan untuk orang dewasa yang lebih muda.[98] Penelitian menunjukkan bahwa faktor-faktor ini juga meningkatkan risiko efek samping pada populasi geriatri ketika diobati dengan SNRI, tetapi tidak dengan SSRI.[99][100] PenelitianTinjauan sistematis yang meneliti kemanjuran antidepresan untuk menghilangkan rasa sakit menyimpulkan bahwa hanya 11 dari 42 perbandingan yang menunjukkan bukti kemanjuran. Tujuh dari sebelas perbandingan termasuk dalam golongan obat SNRI.[101] Referensi
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||