|
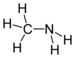
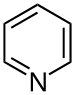
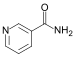
Ikatan karbon–nitrogenIkatan karbon-nitrogen adalah ikatan kovalen antara karbon dan nitrogen dan merupakan salah satu ikatan paling berlimpah dalam kimia organik dan biokimia.[1] Nitrogen memiliki lima elektron valensi dan dalam amina sederhana merupakan trivalen, dengan dua elektron yang tersisa membentuk pasangan elektron sunyi. Melalui pasangan tersebut, nitrogen dapat membentuk ikatan tambahan dengan hidrogen sehingga membuatnya bersifat tetravalen dan dengan muatan positif dalam garam amonium. Banyak senyawa nitrogen dapat berpotensi menjadi basa namun derajatnya bergantung pada konfigurasi: atom nitrogen dalam amida tidak basa karena delokalisasi pasangan elektron sunyi menjadi ikatan rangkap dan dalam pirol pasangan elektron sunyi tersebut adalah bagian dari sekstet aromatik. Serupa dengan ikatan karbon-karbon, ikatan ini dapat membentuk ikatan rangkap dua yang stabil, seperti pada imina, dan ikatan rangkap tiga seperti nitril. Panjang ikatan berkisar dari 147,9 pm untuk amina sederhana menjadi 147,5 pm untuk senyawa C-N= seperti nitrometana menjadi 135,2 pm untuk ikatan rangkap parsial dalam piridin menjadi 115,8 pm untuk ikatan rangkap tiga seperti pada nitril.[2] Suatu ikatan CN sangat terpolarisasi terhadap nitrogen (elektronegativitas dari C dan N adalah masing-masing 2,55 dan 3,04) dan selanjutnya momen dipol molekul bisa tinggi: sianamida 4,27 D, diazometana 1,5 D, metil azida 2,17, piridin 2,19. Karena alasan ini banyak senyawa yang mengandung ikatan CN bersifat larut dalam air. Kelompok fungsional nitrogen
Referensi
|